目前,我国新型煤化工企业发展迅速,主要集中在煤炭资源丰富、水资源短缺的西北地区,耗水量大的同时废水排放量巨大,废水直接排放会破坏水体环境。采煤疏干水主要指煤炭开采过程中井下地质性涌渗水到巷道、为安全生产而排出的自然地下水和井下采煤生产过程中洒水、降尘、灭火灌浆、消防及液压设备产生的废水,据统计我国每年疏干水排放量高达45×108m3。因此,对疏干水进行处理并加以综合利用,不仅可以有效解决耗水量大的问题,同时,经过进一步深度处理后可作为工业用水、农业灌溉用水或地下水补给,避免了水资源的浪费。
疏干水的水质特性主要受地质条件、煤层特性、采煤工艺的影响,主要含有无机盐类、重金属、固体颗粒和微生物等。其中,无机盐类包括SO42-、Cl-、NO3-、Ca2+、Mg2+等。同时,由于煤粉和岩粉渗入水中形成的高悬浮固体(SS),水的颜色一般呈灰色。疏干水一般需要经过一系列的物理、化学和生物处理,才能达到回用标准。但是其中硬度离子的存在(一般在500~2000mg/L之间,以CaCO3计),会增加后续处理系统管道的结垢风险,影响深度处理环节膜的使用寿命。因此,疏干水往往需要先经过软化去除其中的硬度离子后,才能进一步处理与回用。
目前,常用的水体软化方法主要有吸附法、膜分离法、电化学法、化学沉淀法等。其中,吸附法水力停留时间较长,膜分离法适用于低硬度水处理,电化学法需要消耗大量电力,能耗高。而化学沉淀法因其技术成熟、操作简单而被广泛应用,但是会产生大量的含水污泥,需结合压滤单元使用,增加了占地面积和处理成本,在此过程中,悬浮物也得到了同步去除而变成含水污泥。因而,亟须开发一种高效、低耗、短流程的废水硬度处理技术,实现对硬度离子的高效去除,同时降低出水浊度。基于此,课题组研发了核晶造粒(NCP)技术,设计并合成了钙、镁离子专用晶种,开发了一体化装备。具体地,该技术通过预先向装备中投加一定量的专用晶种,调整药剂投加量,使得钙、镁离子分别以碳酸钙、氢氧化镁的形式结晶于专用晶种上,同时通过调整水力学参数,实现对硬度离子和悬浮物的同步去除,并形成致密的造粒体,无需污泥脱水。
以内蒙古某矿业公司采煤疏干水为研究对象,建立了中试处理系统,并采用2级串联的核晶造粒技术,探究不同工艺参数条件下对硬度离子与悬浮物的去除效率,同时对造粒体进行表征分析,揭示核晶造粒同步去除机理,以期为后续的工程应用提供依据。
1、材料与方法
1.1 中试水质
中试在内蒙古乌审旗某矿业公司进行,采煤疏干水经过调节池、斜板沉淀池去除水中大颗粒的沉淀物后进入核晶造粒设备。经测定,pH为8.25±0.13,TDS为(7760±230)mg/L,总硬度(以CaCO3计)为(1310.3±100.5)mg/L,Ca2+为(344±12.5)mg/L,Mg2+为(105.6±10.2)mg/L,HCO3-为(552±20.3)mg/L,浊度为(65.38±8.35)NTU。由于原水pH在8.2左右,因此无需调整pH,可以直接进入核晶造粒反应器。
1.2 试验材料
中试中,一级使用钙、镁专用复合晶种,二级使用镁专用晶种,两种晶种的初始粒径均为80~120目(0.15~0.2mm),因此具有较大的比表面积,这为Ca2+/Mg2+的附着成核提供了更多位点。其中,钙专用晶种的堆密度约为1.5g/cm3,镁专用晶种的堆密度约为1.2g/cm3,高密度的晶种提高了其耐冲击负荷的能力,同时能够快速沉降。由于原水中含有大量的HCO3-,因此,第一级与第二级核晶造粒均使用NaOH作为诱晶剂。
1.3 中试装置
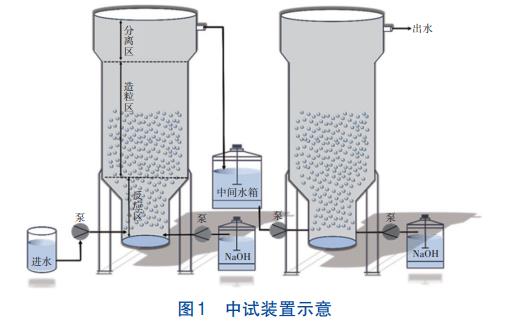
现场中试装置如图1所示,反应器主体由SS304不锈钢加工而成,总高为6.0m,由底部至顶部分为反应区(1.2m)、造粒区(3.0m)和分离区(1.8m);设备底部设有进水口和进药口。在泵的作用下原水进入第一级反应器,同时进药泵将NaOH送入反应器除钙,第一级反应结束后出水进入中间水箱,再经由泵进入第二级反应器,同时加入NaOH用以除镁。反应结束后,调节出水pH至中性。中试过程中,第一级处理能力为22m3/h,第二级处理能力为10m3/h。部分第一级出水被回流至原有水处理系统,对中试不产生影响。
1.4 分析仪器与方法
pH:奥豪斯ST3100型pH计;总硬度、钙、镁离子:国标EDTA滴定法;浊度:哈纳HI93703-11浊度仪,直接测定出水;造粒形貌及元素分布表征:德国ZEISSSigma300SEM能谱仪(SEM);表面基团、晶型结构分析:日本岛津IRTracer100型傅里叶漫反射红外光谱仪(FT-IR)、美国ThermoScientificESCALABXi型X射线光电子能谱仪(XPS)和德国BrukerD8Advancee型X射线衍射仪(XRD);造粒体粒径:英国马尔文Mastersizer2000型激光粒度仪。钙、镁离子去除率的计算方法如下:
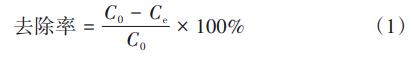
式中:C0为进水钙、镁离子浓度;Ce为出水经调整成中性后的钙、镁离子浓度。
2、结果与讨论
2.1 核晶造粒技术对钙、镁离子的去除率
两级串联核晶造粒技术对钙、镁离子的去除效果及浊度影响见图2。
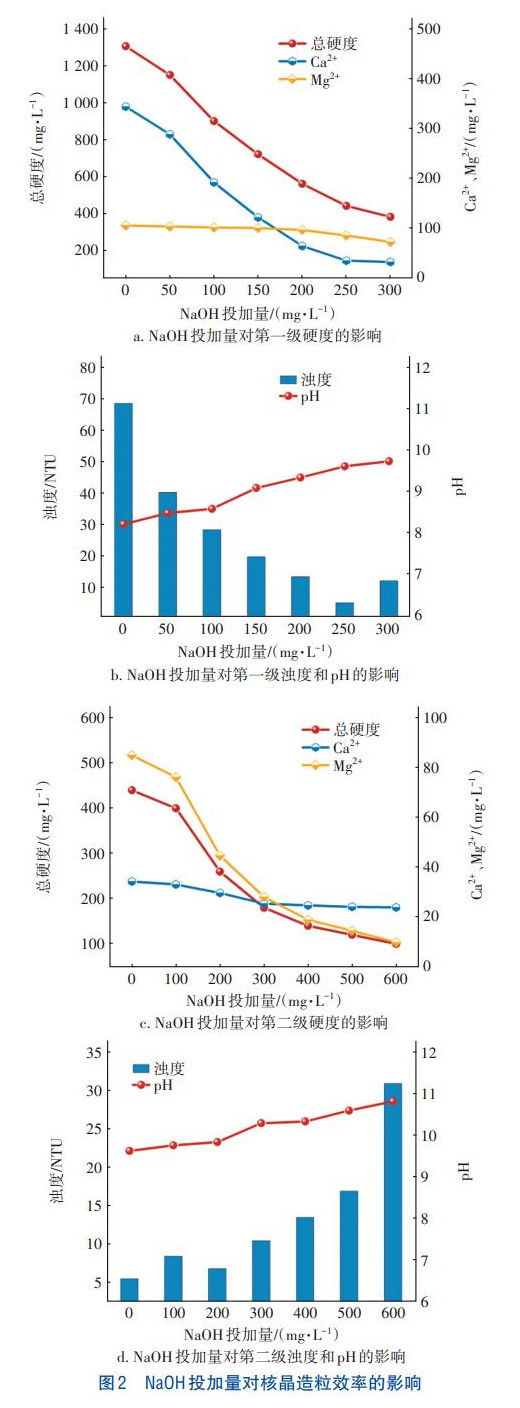
当废水中的离子浓度积大于CaCO3的溶度积(Ksp)时,CaCO3会因为过饱和而结晶析出,Mg(OH)2也是如此。因此,过饱和度是驱动离子结晶析出的主要动力。由于原水中存在约550mg/L(9.01mmol/L)HCO3-,理论上与NaOH反应能够生成9.01mmol/LCO32-,可与约360mg/L的Ca2+反应生成CaCO3,因此,第一级核晶造粒反应器中无需额外加入Na2CO3。如图2(a)所示,随着NaOH投加量的增加,总硬度和Ca2+浓度呈现明显下降趋势,但是Mg2+浓度下降不明显。这是由于此时NaOH与HCO3-反应生成了CO32-,进而与Ca2+反应生成CaCO3而结晶于钙专用晶种上。而此时的pH及NaOH投加量不足以达到Mg(OH)2沉淀的过饱和度。因此Mg2+的去除可能是由于共沉淀作用。
由图2(b)可知,随着NaOH投加量的增加,出水浊度先降低后增加,当NaOH投加量为250mg/L时浊度达到最低(5.6NTU),此时对总硬度、Ca2+、Mg2+和浊度的去除率分别为66.3%、90.1%、19.0%和91.8%。当投加量继续增加至300mg/L时,总硬度、Ca2+和Mg2+的去除率仍在增加,但出水浊度明显上升,这是由于生成的CaCO3和Mg(OH)2并未结晶附着于钙专用晶种上,而是随出水流出。
由图2(c)可知,随着NaOH投加量的增加,对总硬度和Mg2+的去除效果明显提高,这是由于此时主要生成了Mg(OH)2结晶并附着于镁专用晶种上。钙离子则由于共沉淀作用而被少量去除。但是不同于第一级核晶造粒,随着NaOH投加量的增加,出水浊度呈现逐渐上升趋势,这可能是水中存在少量Ca2+,影响了Mg(OH)2的附着,导致出水浊度上升。因此,综合考虑出水硬度(<200mg/L)与浊度,确定第二级核晶造粒的加药量为500mg/L。事实上,将出水调节至中性后,总硬度约为140mg/L,能够满足出水之于硬度要求。最终,经由第一、第二级核晶造粒处理后,总硬度、Ca2+、Mg2+和浊度的去除率分别达到了91.1%、93.1%、86.3%和75.3%。
2.2 晶种填充质量、上升流速对出水水质的影响
不同晶种用量下,各指标的去除效果见图3。
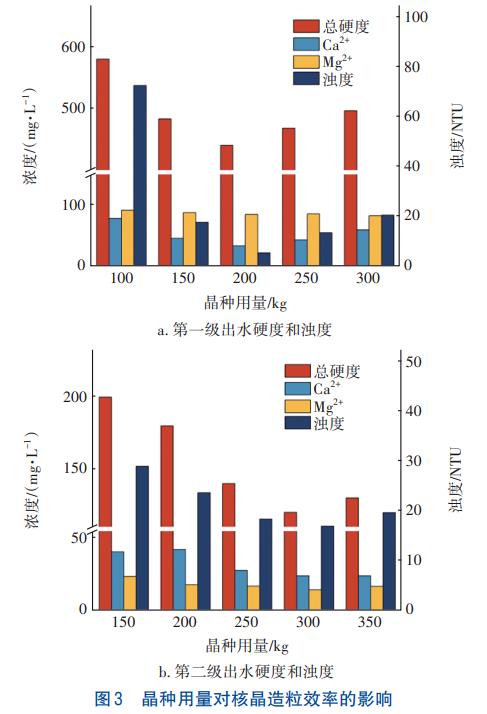
在第一级核晶造粒设备中,随着专用晶种用量的增加,出水硬度、Ca2+浓度和浊度均呈现先减小后增加的趋势,而Mg2+浓度几乎没发生变化。当晶种用量为200kg时,出水效果达到最佳。分析原因,当晶种用量少于200kg时,其结晶能力不足以吸附全部CaCO3/Mg(OH)2颗粒,导致出水浊度较高;而当晶种用量>200kg时,由于进水上升流速一定,晶种流化状态变差,进而降低了晶种与CaCO3/Mg(OH)2的接触面积,导致出水浊度升高。同样,确定第二级核晶造粒的最佳晶种用量为300kg。
除此之外,水力条件也会影响污染物在晶种表面的附着。由于中试设备的尺寸是固定的,因此通过调整进水流量可改变其上升速度,进而影响污染物与晶种的接触时间和接触面积、晶种的流化状态以及系统的混合强度。不同上升流速下,对总硬度、Ca2+、Mg2+和浊度的去除效果见图4。
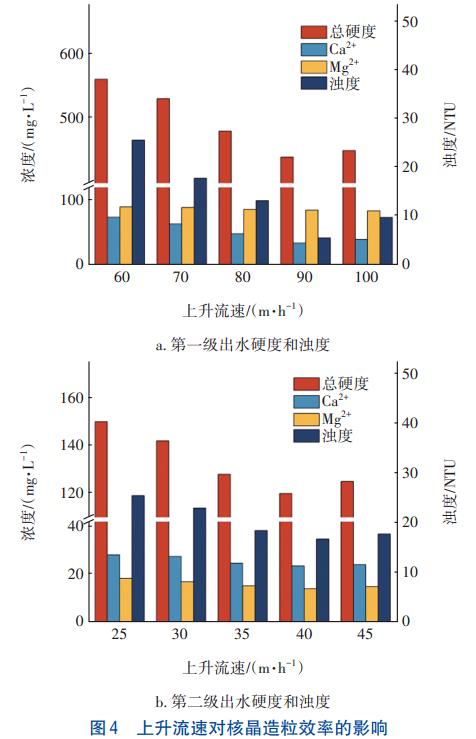
由图4(a)可知,当上升流速为90m/h时,出水浊度达到最低值,而大于或小于90m/h时出水浊度均升高。分析原因,当上升流速较小时,专用晶种不能达到最佳流化状态,导致晶种暴露位点少,难以使CaCO3/Mg(OH)2全部附着于晶种上,随水流流出从而增加了出水浊度。而过高的上升流速,虽然会使晶种的流化状态变得更好,但减少了晶种与污染物的接触时间,并会冲刷晶种表面的附着物,导致出水浊度升高。同样,确定第二级核晶造粒的最佳上升流速为40m/h。
2.3 连续稳定运行效果
在分别探究了第一、第二级核晶造粒的影响因素基础上,进行了72h的连续流试验,以验证系统的稳定性及耐冲击负荷能力。其间每隔4h测定进水和第二级核晶造粒出水的总硬度、浊度和pH,结果表明,进水平均总硬度和浊度分别为1358.9mg/L和59.3NTU,而第二级出水的分别为140.2mg/L和18.4NTU,去除率分别为89.7%和68.9%。值得注意的是,在连续运行过程中,进水的总硬度及浊度波动较大,但是出水总硬度能够满足小于200mg/L的要求,同时出水浊度波动较小,出水pH平均值为10.58。因此,可以肯定的是,两级串联的核晶造粒系统能够同步去除废水中的硬度和浊度,并表现出优异的性能及稳定性。
2.4 造粒体形貌、组成及表面特性分析
在经过连续72h运行后,分别取出第一、二级核晶造粒装置底部的造粒体,用以分析造粒体的结构特征。XRD分析结果显示,第一级造粒体在2θ为26.2°、27.2°、33.1°、37.9°、46.5°、48.9°、51.9°、53.0°和53.9°处呈现出明显的衍射峰,与CaCO3的特征衍射峰精准吻合(JCPDS#76-0606),且无其他杂峰,这表明在第一级核晶造粒装置中形成了较纯的CaCO3造粒体。同样地,第二级造粒体在2θ为18.5°、37.9°、50.7°和58.6°处呈现出明显的衍射峰,这与Mg(OH)2的特征衍射峰吻合(JCPDS#84-2163),表明在第二级核晶造粒装置中形成了Mg(OH)2造粒体。除此之外,Mg(OH)2造粒体XRD图中出现了明显的专用晶种的特征衍射峰,这是因为第二级原水中的Mg2+浓度较低,生成的Mg(OH)2含量低,并未完全覆盖专用晶种。
第一级和第二级核晶造粒体在不同倍数下的SEM和EDS照片见图5。可以看出,第一级的CaCO3造粒体粒径分布均匀,粒径大约为1.0mm,这证明废水中的Ca2+已经以CaCO3的形式附着并生长于专用晶种表面(晶种粒径约为0.2mm),并促使晶种长大。研究表明,CaCO3晶体表面光滑,具有规则的斜方体或球形结构。但是,第一级中的CaCO3造粒体表面呈现粗糙状,附着了不规则的物质,这是由废水中的悬浮物被同步去除所导致的。同样地,第二级中的Mg(OH)2造粒体表面也附着了悬浮物,但是由于Mg2+含量较少,因此其造粒体仅是部分呈现规则状,而且并未长大。从EDS照片可以看出,CaCO3造粒体表面含有Mg元素,而Mg(OH)2造粒体表面含有Ca元素,这是由于发生了共沉淀作用,使得Mg2+和Ca2+分别沉淀于CaCO3和Mg(OH)2造粒体表面。

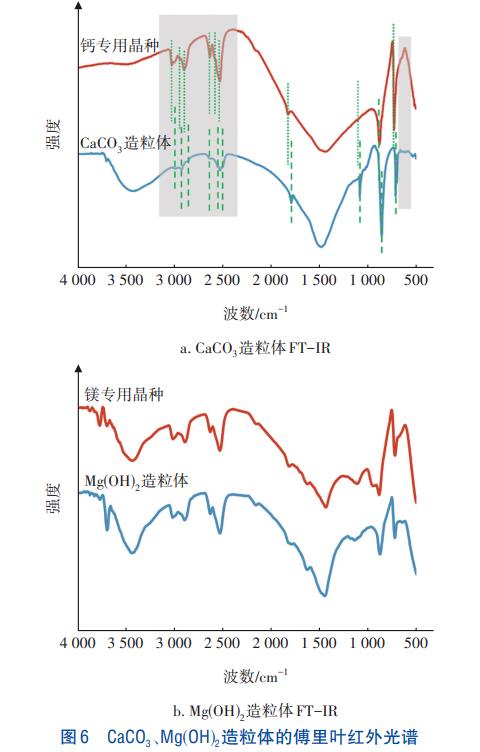
图6呈现了第一级和第二级核晶造粒体的傅里叶红外光谱(FT-IR)。如图6(a)所示,可以明显观察到钙专用晶种的衍射峰均已经被CaCO3造粒体的衍射峰覆盖,这证明了废水中的CaCO3已经生长在钙专用晶种表面,并促进其生长,这与XRD结果一致。同时可以观察到,相比于钙专用晶种,CaCO3造粒体在2500~3000cm-1和500~750cm-1处的衍射峰相对平整且更光滑,这是由于悬浮物的嵌入使得CaCO3基团排列不规则,以致相邻峰相连而合并,促使吸收带数目减少,成为一些宽而钝的带。这表明废水中的悬浮物被同步去除,除被表面吸附外,也嵌入CaCO3造粒体中,这与SEM结果一致。但是,同样的结果并未出现在镁专用晶种和Mg(OH)2造粒体的FT-IR图中,这也间接证明了镁造粒体由于Mg2+含量少,而并未促使专用晶种长大,因此二者的FT-IR图并没有明显变化。
对第一、第二级造粒体的粒径分布测定结果显示,CaCO3造粒体的d10、d50、d90分别为664.7、902.2、1322.6μm,明显大于专用晶种(0.15~0.2mm),证明了专用晶种长大。相反,Mg(OH)2造粒体的相应值分别只有117.4、228.9、395.2μm,仅略大于镁专用晶种。这也与SEM结果一致。但是,如果长期运行,Mg(OH)2最终会促使镁专用晶种长大,从而使得Mg2+从废水中去除。
分别取CaCO3、Mg(OH)2造粒体,测定其X射线光电子能谱(XPS),用以进一步了解造粒体的表面化学成分,结果如图7所示。对于CaCO3造粒体,XPS的扫描结果证实了C、O、Ca和Mg的存在。图7(a)中,C1s的高分辨率分峰拟合结果显示了三个碳酸盐相关的峰值。其中284.8eV处观察到了C—C/C=O的峰,可能是废水中的有机物被吸附于造粒体上所致,这一点已被先前的研究证实。289.7eV处的结合能峰对应于碳酸盐的峰,286.3eV处的峰则代表了残余含氧基团中的C—O。类似地,O1s可以被拟合为三个峰,见图7(b)。其中,位于533.3eV处的峰代表了O—H/C—O—C;位于531.9eV处的峰代表了CaCO3造粒体中的CO32-;而位于530.9eV处的峰则代表了HO—Mg,这表明其造粒体表面存在Mg。
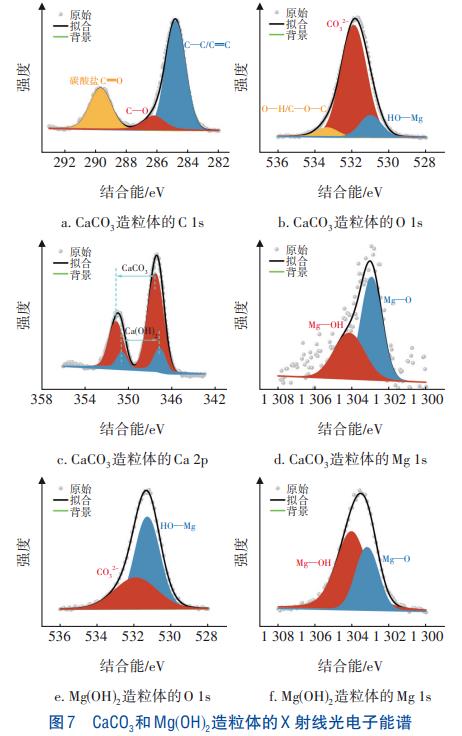
在图7(c)中Ca2p峰可以被分别拟合为位于315.2、347.5eV的CaCO3以及位于350.6、347.1eV的Ca(OH)2,原因可能是NaOH的投加导致生成了Ca(OH)2。Mg1s可以被拟合为位于1304.2eV的Mg—OH峰以及1302.9eV的Mg—O峰,这证明了CaCO3造粒体表面存在Mg(OH)2,但是因为其含量较少而未在XRD中体现。在图7(e)中,Mg(OH)2造粒体的O1s可以被拟合为两个峰,分别是位于531.9eV处的CO32-峰和531.3eV处的HO—Mg峰,原因可能是水中残余的CO32-导致Mg(OH)2造粒体表面存在CO32-。而Mg1s可以被拟合为位于1304.2eV处的Mg—OH峰及位于1302.9eV处的Mg—O峰,证明了造粒体的主要成分为Mg(OH)2。因此,经过对核晶造粒体的系列表征,可以确定废水中的Ca2+、Mg2+以及悬浮物被同步去除,而且分别在第一级和第二级核晶造粒装置中形成了密实的CaCO3、Mg(OH)2造粒体。
2.5 核晶造粒机理分析
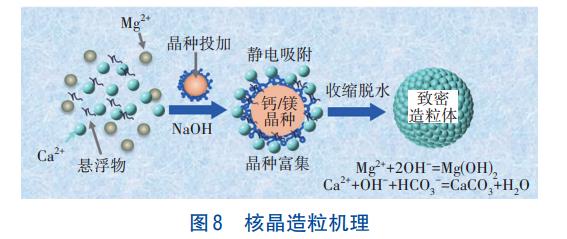
基于上述表征分析,废水中Ca2+、Mg2+的核晶造粒去除机制见图8。首先,对专用晶种表面Zeta电位进行了分析,当pH为3.2、6.8、8.9、9.8、10.6、11.8时,钙专用晶种表面Zeta电位分别为5.3、-6.2、-7.6、-5.5、-8.3、-9.6mV;当pH为3.2、5.8、7.8、9.5、10.9、11.2、11.5时,镁专用晶种表面Zeta电位分别为4.6、1.3、-9.8、-13.5、-14.9、-16.8、-18.3mV。可见,在pH>8时钙、镁专用晶种表面均带负电。因此在第一级核晶造粒装置中,当晶种充分流化后,废水中的Ca2+由于静电吸附作用,聚集于专用晶种上,此时,加入的NaOH提供了大量的OH-,并快速与原水中的HCO3-反应生成CO32-,与吸附于专用晶种上的Ca2+反应生成CaCO3,进而促使专用晶种长大,在此过程中裹挟了废水中的悬浮物,促使其同步去除。而当专用晶种被覆盖后,其表面为新生成的CaCO3,且新生成的CaCO3表面仍带负电荷,因此会吸附Ca2+附着,如此循环使得专用晶种随着运行时长而长大,并在水力作用下密实化。不同的是,在第二级核晶造粒装置中,初始由于静电作用,Mg2+被吸附于专用晶种表面,NaOH的加入使得Mg(OH)2处于过饱和状态,从而在晶种表面不断进行富集,并促使其长大。而当Mg(OH)2包裹专用晶种后,由于新生成的Mg(OH)2表面为正电荷,此时会吸附水中的OH-,进而促进镁离子聚集,最终使得其长大并密实化。
3、结论
①两级串联核晶造粒技术可高效去除疏干水中的Ca2+、Mg2+,当一级NaOH投加量为250mg/L、上升流速为90m/h、晶种用量为200kg,二级NaOH投加量为500mg/L、上升流速为40m/h、晶种用量为300kg时,总硬度去除率接近90%,浊度去除率为68.9%。同时,在连续运行中去除效果较稳定。
②结合XRD、XPS、SEM-EDS、FT-IR等表征可以发现,分别在第一级和第二级核晶造粒装置中形成了密实的CaCO3、Mg(OH)2造粒体。由于悬浮物的存在,晶种表面更加粗糙,并使造粒体FT-IR发生红移;在过饱和度、水力剪切的作用下,于专用晶种表面发生非均相成核,促使晶种长大。
③通过Zeta电位表征,在高pH时晶种表面均带负电,初期能够有效吸附Ca2+、Mg2+,在药剂的作用下产生CaCO3、Mg(OH)2并生长于晶种表面;随后由于新生成的CaCO3、Mg(OH)2的表面电荷不同,后续晶种持续长大的机理不同,但最终均能够去除废水中的Ca2+、Mg2+。
④相比于传统的化学沉淀/高密度沉淀池除硬而言,核晶造粒技术具有水力停留时间短的优点。因为核晶造粒装置为竖向,节省了占地面积;同时,由于最终生成了含水率更低且密实的CaCO3、Mg(OH)2造粒体,无需后续污泥处理,节省了整体的运行费用。(来源:西安交通大学人居环境与建筑工程学院,中科核润<陕西>生态环境有限公司,陕西水务发展集团有限公司,江苏新宇天成环保有限公司)



