镍是生命必须的微量元素,但过量的镍会危害环境和人体健康。镍污染主要来源于钢铁制造、电镀、电子等行业产生的漂洗水。根据《电镀污染物排放标准》(GB21900—2008),电镀废水在排入水体前,总镍不超过0.1mg/L。因此,如何高效深度去除电镀废水中的镍是非常重要的。
目前,离子交换、膜分离法、化学沉淀法等在处理含镍废水领域应用广泛,但仍有许多不足,如产生二次污染、操作条件严苛、再生能力差等。吸附技术被认为是处理废水中镍污染最实用的方法之一,它操作简便、吸附能力强、应用成本低。吸附法的核心是吸附剂的选择,只有吸附容量大、稳定性好、低成本、易再生的吸附剂才能有广阔的工程应用前景。壳聚糖(CTS)是从甲壳类动物外壳、真菌、昆虫外骨骼等多种生物源中提取的多糖类聚合物,含有—NH2、—OH等活性基团,易与Ni(Ⅱ)形成配合物,将镍从水溶液中去除。然而,CTS耐酸性和韧性差,实际应用中需要对其进行改性处理。沸石、生物炭、硅藻土有被报道应用于CTS复合材料制备。沸石属于硅酸盐类晶体,硅和铝能通过微孔孔道和空腔形成三维晶体结构。沸石分子筛(ZSM-5)是人工合成的沸石,具有稳定的硅铝比和强大的离子交换容量。
本文主要研究CTS-沸石(CTS-Z)对低浓度镍离子的深度吸附作用。通过静态吸附实验得到溶液pH和吸附剂投加量的最佳值,并拟合分析吸附动力学和热力学模型。利用动态吸附实验考察CTS-Z的可再生能力,以预测其在实际工程应用中的可能性。
1、实验材料与方法
1.1 主要实验材料
CTS(脱乙酰度大于90%)、ZSM-5、Ni(NO3)2·6H2O、乙酸、NaOH、HCl。
1.2 CTS-Z微球的制备
3.0gCTS粉末溶于2%(体积分数)的乙酸溶液中,每100mL该溶液中加入1.5gZSM-5粉末,40℃下搅拌1h。将混合溶液滴加到1mol/L的NaOH溶液中固化3h,转入150℃高压釜中水热交联12h得到CTS-Z微球,之后用超纯水洗至中性,烘干备用。
1.3 静态吸附除镍实验
将5.0gNi(NO3)2·6H2O溶于1L超纯水中制得1g/LNi(Ⅱ)原液,根据需求配置相应浓度的镍溶液。
在100mL锥形瓶中加入50mL10mg/L的镍溶液,用0.1mol/L的NaOH或HCl溶液调节pH至8,以1.00g/L投加量投加CTS-Z微球,30℃、200r/min条件下振荡吸附24h,取2mL水样经过0.45μm水系滤膜过滤后测定总镍浓度。同时,改变溶液pH、吸附剂投加量、时间和温度等条件进行探究。
1.4 动态吸附除镍实验
实际电镀含镍废水取自某电子产业园,出水总镍为8.93mg/L,调节实际废水pH为8,采用上流式进水方式,在高30cm、内径1.5cm的玻璃吸附柱中装填厚度10cm的CTS-Z微球,流速设为15mL/min,3次吸脱附实验考察CTS-Z对Ni(Ⅱ)连续流吸附性能。
2、实验结果与讨论
2.1 溶液pH的影响
因为当pH超过8时,Ni(Ⅱ)会以Ni(OH)2的形式析出,所以实验中控制pH为2~8。CTS-Z对Ni(Ⅱ)的吸附量随着pH的增加而增加(见图1)。这是因为酸性条件下,溶液中的H+与Ni(Ⅱ)争夺CTS-Z表面的吸附位点,降低了Ni(Ⅱ)的吸附能力。随着pH的升高,H+浓度降低,竞争吸附减弱;同时,CTS-Z的官能基团—OH、—COOH被去质子化,导致CTS-Z表面带负电荷,与带正电荷的Ni(Ⅱ)通过静电引力相互作用。因此,后续实验中Ni(Ⅱ)溶液的pH设置为8。
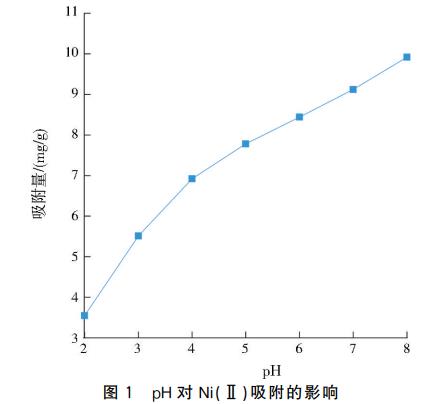
2.2 吸附剂投加量的影响
当CTS-Z微球投加量从0.25g/L增加到2.00g/L时,Ni(Ⅱ)去除率从72.04%逐渐提高到99.96%,而吸附量从28.816mg/g降低到3.324mg/g(见图2)。这一结果可用吸附位点理论来解释。当溶液中Ni(Ⅱ)浓度保持不变,CTS-Z微球表面吸附位点数与吸附剂投加量成正比,投加量增加,CTS-Z对Ni(Ⅱ)的吸附能力和去除效率也增强。但单位吸附剂所承担的吸附任务减少,因此单位吸附剂的吸附容量会相应减小。基于以上分析,后续实验吸附剂投加量设为1.00g/L。
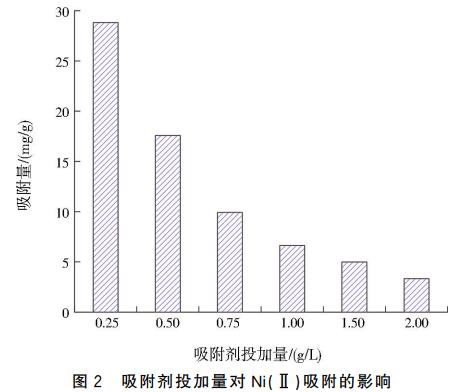
2.3 吸附动力学和吸附等温线拟合分析
CTS-Z的吸附动力学和热力学模型拟合如图3所示。整个吸附过程分为3段,分别是快速表面吸附阶段(0~60min)、慢速内扩散阶段(60~240min)和微孔吸附平衡阶段(240min后),这是因为金属离子与CTS-Z微球体内活性位点之间存在很强的吸引力,反应初期Ni(Ⅱ)能快速扩散到CTS-Z的内部层间结构,反应后期,越来越多的活性位点被占据,反应速率下降,最终达到平衡状态,平衡吸附量为9.9938mg/g。通过拟合曲线得到吸附动力学参数:准一级动力学,理论平衡吸附量为9.7193mg/g,系数为0.0167g/(mg·min),R2为0.9830;准二级动力学,理论平衡吸附量为11.9543mg/g,系数为0.0014g/(mg·min),R2为0.9932。准二级动力学的R2更大,更适合描述CTS-Z微球对镍的吸附过程,说明CTS-Z吸附镍主要依靠化学作用。
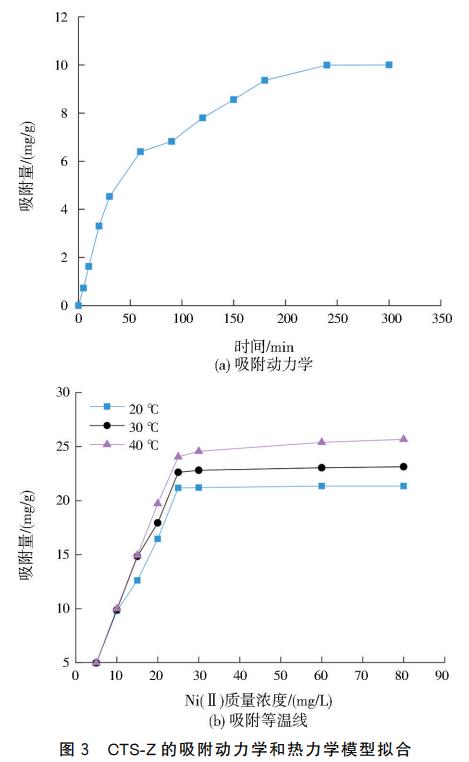
在不同温度(20、30、40℃)下,CTS-Z对Ni(Ⅱ)的吸附等温线均呈现快速上升—平台稳定趋势,当Ni(Ⅱ)达到25~30mg/L时,3条吸附等温线均进入平台区,表明此时吸附剂表面活性位点趋于饱和。相同Ni(Ⅱ)浓度下,温度越高,CTS-Z对Ni(Ⅱ)的吸附速率越快,平衡吸附量越高,这说明吸附剂的饱和吸附量与温度有强相关性,在一定范围内温度越高越有利于吸附进行。相同温度下,Langmuir模型(R2为0.8593~0.9657)拟合效果比Freundlich模型(R2为0.6910~0.7191)好,说明CTS-Z对Ni(Ⅱ)的吸附更符合Langmuir模型,属于单分子层均匀吸附,且吸附过程是化学吸附同时存在物理吸附。
2.4 表征分析
2.4.1 扫描电子显微镜(SEM)、比表面积和孔径分析
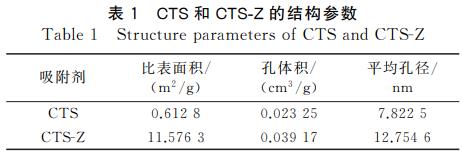
CTS和CTS-Z的SEM图见图4。CTS微球具有平坦且光滑的表面。相反,CTS-Z微球表面呈现出多孔且粗糙的形态,并且表面附着有细丝状物质,说明ZSM-5分子已成功负载到CTS上。CTS和CTS-Z的结构参数如表1所示。ZSM-5的引入显著提升了CTS的比表面积,CTS的比表面积为0.6128m2/g,与ZSM-5交联改性后大幅增加至11.5763m2/g。这一显著增长归因于ZSM-5分子骨架作为支撑结构,有效增加了CTS的孔隙度,提高其吸附效率。根据吸附/解吸曲线分析,CTS和CTS-Z均展现出介孔材料的特性,有利于吸附的发生。

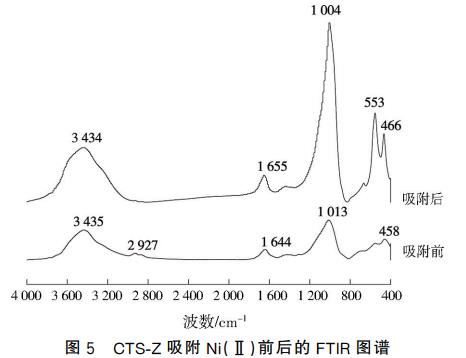
2.4.2 傅里叶红外光谱(FTIR)分析
由图5可知,吸附Ni(Ⅱ)后,CTS-Z的峰值强度发生了变化。吸附后3435cm-1处的—NH2和—OH伸缩振动峰向低频段偏移,且由窄峰变为宽峰,表明—NH2和—OH参与Ni(Ⅱ)的吸附过程;2927cm-1处—CH伸缩振动峰消失,可能是CTS-Z微球与Ni(Ⅱ)产生氢键,消耗了—CH振动峰;553cm-1处的峰是Ni—OH—Ni伸缩振动产生的;1013、458cm-1处峰值强度增加,说明吸附Ni(Ⅱ)破坏了ZSM-5的空腔结构,可能是与空腔中的Na+、K+等发生离子交换作用。
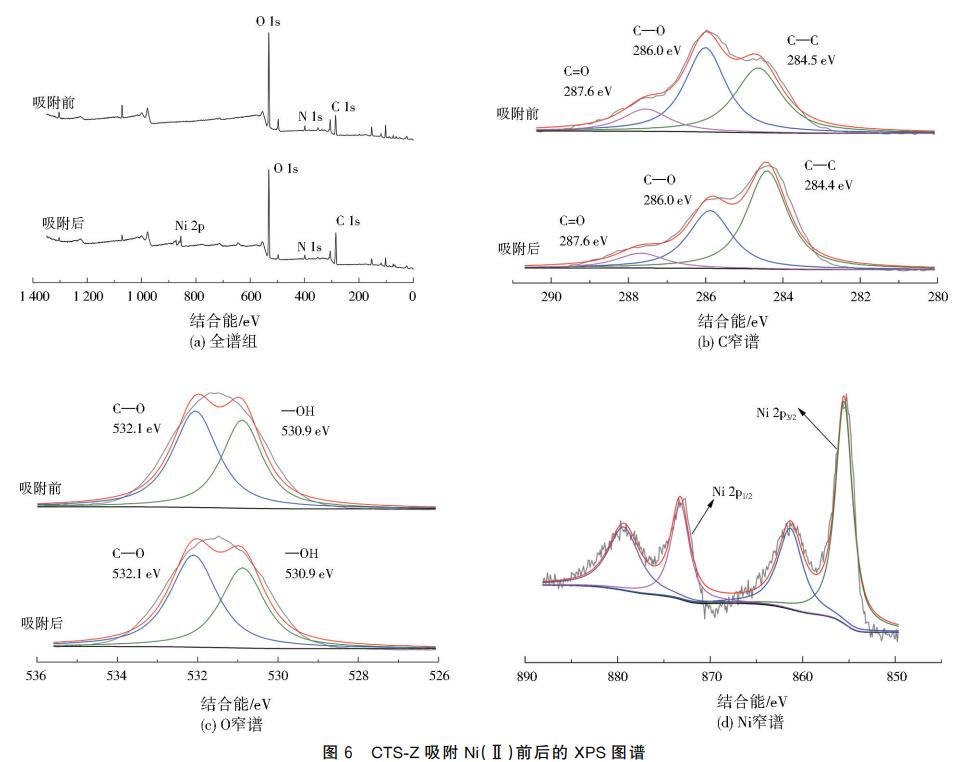
2.4.3 X射线光电子能谱(XPS)分析
为更深入了解改性后材料表面的化学组成及其对Ni(Ⅱ)的吸附机理,对CTS-Z吸附Ni(Ⅱ)前后进行了XPS表征,结果见图6。吸附Ni(Ⅱ)后的CTS-Z全谱中出现了明显的Ni特征结合能峰,表明Ni(Ⅱ)已成功吸附在CTS-Z上;吸附后,CTS-Z表面的Na+消失,说明Ni(Ⅱ)与CTS-Z表面的Na+发生了阳离子交换反应。CTS-Z在吸附前后,C窄谱上均出现3个特征峰,分别代表着C—C、C—O和C=O的化学键结构;吸附后,C—C特征峰的面积从原先的40.6%显著提升至55.4%,这一变化可能因为吸附过程中CTS分子链发生伸展或重新排列,使得原本被遮蔽在材料内部的C—C暴露出来,进而表现为C—C特征峰强度的增加;C—O特征峰的面积从45.6%下降至34.7%;C=O特征峰面积从13.8%下降到9.9%,主要是因为CTS-Z表面部分—OH与Ni(Ⅱ)发生配位或螯合作用,反映在XPS图谱上,即特征峰面积减小;另外,ZSM-5与CTS交联时其表面的活性位点与CTS上的—OH有反应关系,也会影响C—O特征峰面积。吸附后代表—OH的特征峰相对强度有所减少,也证明了—OH参与了吸附Ni(Ⅱ)反应。Ni2p3/2和Ni2p1/2的峰结合能在856.50、873.80eV附近,其中Ni2p1/2的峰反映了络合氧化镍的特征,表明Ni(Ⅱ)在CTS-Z中与—OH相互作用。
2.5 CTS-Z吸附Ni(Ⅱ)的机理研究
通过以上表征和吸附实验分析可知,CTS-Z对Ni(Ⅱ)的吸附涉及多种机制,主要包括表面络合、离子交换和静电相互作用。Ni(Ⅱ)能与CTS-Z表面的—NH2和—OH形成配位络合物去除;与CTS-Z骨架上的Na+、K+等发生离子交换反应去除;在碱性条件下,Ni(Ⅱ)还可通过静电相互作用被吸附到带负电的CTS-Z上去除。吸附过程主要包括以下反应:
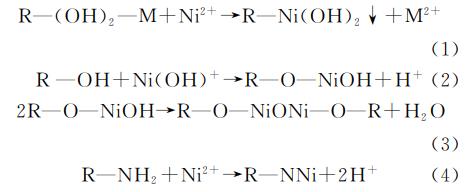
2.6 CTS-Z的动态吸附实验分析
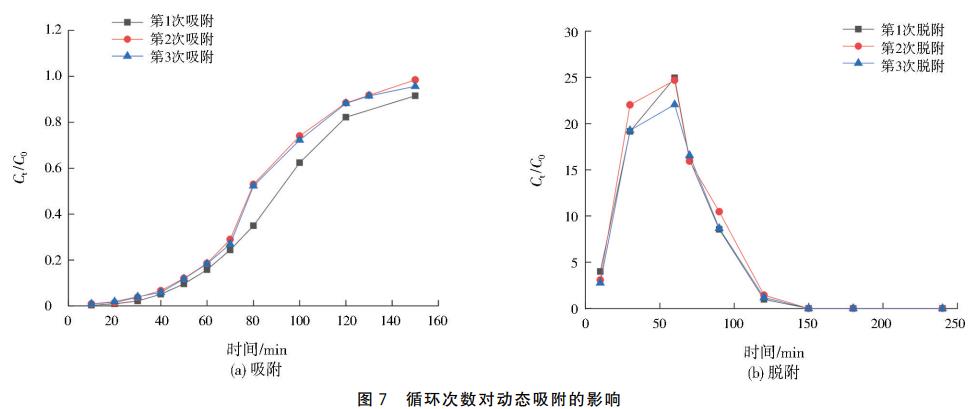
因为总镍不超过0.1mg/L,所以本实验设置Ni(Ⅱ)反应后和初始质量浓度比(Ct/C0)为0.01对应的时间为穿透点。吸附柱运行初期,出水Ni(Ⅱ)浓度缓慢增加(见图7(a)),这是因为吸附剂表面有着大量的吸附位点,对Ni(Ⅱ)的吸附性能优异;但随着时间的延长,CTS-Z表面的吸附位点被逐渐占据,底层吸附位点趋于饱和,吸附带上移,导致吸附柱对进水Ni(Ⅱ)的吸附能力减弱。第1、2、3次吸附的穿透时间分别为20、10、10min,与第1次吸附相比,第2、3次吸附穿透时间提前,可能是脱附不彻底,导致CTS-Z的吸附位点没有充分恢复。第1、2、3次吸附的吸附量分别为2.4425、1.2208、1.2205mg/g,下降幅度不大,说明CTS-Z在连续3次吸附后仍具有良好的吸附性能和稳定性。以1.0mol/L的HCl脱附,随着时间的延长,第1、2、3次脱附的出水Ni(Ⅱ)呈现先升后低的趋势(见图7(b)),均在60min时最高,且在150min内完成脱附,脱附率分别为94.07%、92.08%、89.77%,说明HCl脱附效果良好。综合3次CTS-Z的吸脱附结果,发现CTS-Z有代替离子交换树脂作为实际电镀含镍废水中深度处理的吸附材料的潜力。
3、结语
采用水热交联法成功制备出CTS-Z微球,旨在探索其作为新型替代离子交换树脂的材料应用于电镀含镍废水处理中的可行性。
1)当溶液pH为8、CTS-Z投加量为1.00g/L时,30℃下吸附240min后,CTS-Z对Ni(Ⅱ)的吸附量达到平衡,平衡吸附量为9.9938mg/g。CTS-Z对Ni(Ⅱ)的吸附行为遵循准二级动力学和Langmuir模型,这表明吸附过程主要受化学和物理吸附限制。
2)SEM、比表面积和孔径分析表明,CTS-Z微球表面呈现出粗糙且多孔的结构特性。FTIR和XPS分析表明,—OH、—NH2等基团参与了Ni(Ⅱ)的吸附过程。
3)动态除镍实验中,CTS-Z对Ni(Ⅱ)的吸附量从第1次吸附的2.4425mg/g降至第3次吸附的1.2205mg/g,3次脱附的脱附率始终保持在89%以上,说明CTS-Z有良好的除镍能力和再生能力,在深度除镍领域有很好的工程应用前景。(来源:合肥工业大学资源与环境工程学院,安徽美自然环境科技有限公司)



